희토류 형광체의 발광특성 및 대체/저감 기술 개발
김 영 국_ 한국기계연구원 부설 재료연구소 선임연구원
Ⅰ. 서 론
희토류 원소는 반도체, 디스플레이, 자동차 등 대부분의 전기전자, 운송, 유리, 세라믹 생산품에 광범위하게 사용되고 있으며 특히 최근에는 고효율 조명, 전기자동차, 풍력발전 등에 사용되는 자성체, 전지, 형광체 등 청정에너지 관련 각종 고기능성 소재에 희토류 원소가 첨가되어 에너지 효율과 성능을 높이는데 있어 핵심적인 역할을 하고 있다.
또한 석유 개질을 위한 촉매제, 고강도 구조재료, 유리의 발색재 등 다양한 영역에서 희토류 원소가 핵심적인 역할을 하고 있어 심지어 희토류 수입량이 첨단산업 발달에 대한 척도로 인용될 정도로 희토류 원소는 첨단산업에 필수적인 요소이다.
희토류 원소 응용 제품 중에서도 형광체는 희토류 관련 소재 중 단위 중량당 단가가 가장 비싼 소재이다. 따라서 희토류 분야에서 형광체는 전체 희토류 사용량의 7%가량이지만 금액으로 보면 전체 희토류의 30%가 형광체 분야에 소모되고 있다.
형광체에는 Eu, Tb, Gd 등 고가의 중(重)희토류 원소가 빛을 발생시키는 활성제로 주로 사용되고 있으며 Y, La, Ce 등이 모체 소재로 사용되고 있다. 일부 희토류가 없는 조성도 사용되고 있으나 전체에서 차지하는 부분은 그리 크지 않은 실정이다.
따라서 최근 희토류 수급 문제로 인한 가격 상승은 형광체 분야에도 큰 파장을 일으키고 있어 이에 대한 대책이 시급하다. 특히 형광체에 많이 사용되고 있는 Eu, Tb 등 중희토류 원소들은 수급의 위험성이 큰 대표적인 원소들로써 향후에도 급격한 가격 변동의 가능성이 크다. Eu의 경우 2007년 300불/kg 정도의 가격이 2011년 말에는 3800불/kg으로 10배 가까이 치솟았다.
이에 따라 2011년에는 냉음극 형광등용 형광체의 수입 가격은 수년 전에는 80불/kg이었던 것이 희토류 가격 상승으로 800불/kg까지 치솟았다. 그 결과 일부 제품의 경우 형광등 가격이 3배 가까이 치솟았다 (Philips Lighting, 2011).
이와 같이 희토류 관련 산업에서 형광체 분야의 중요성은 매우 크며 안정적인 산업기반 확보를 위해서는 희토류 원소의 사용량 저감이나 재활용 기술에 대한 연구가 필요하며 궁극적으로는 완전한 대체가 요구된다.
본고에서는 형광체 분야에서 희토류 원소 사용 현황을 살펴보고 현재 진행되고 있는 희토류 원소의 대체, 저감 기술 연구 현황에 대해 알아보고자 한다.
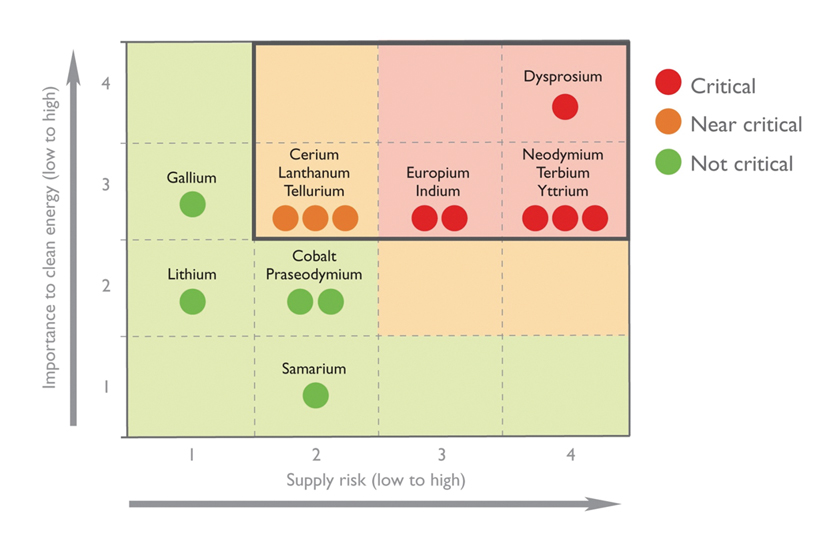
그림 1. 희토류 원소별 수급 문제 (U.S Department of Energy 2010 Critical Materials Strategy)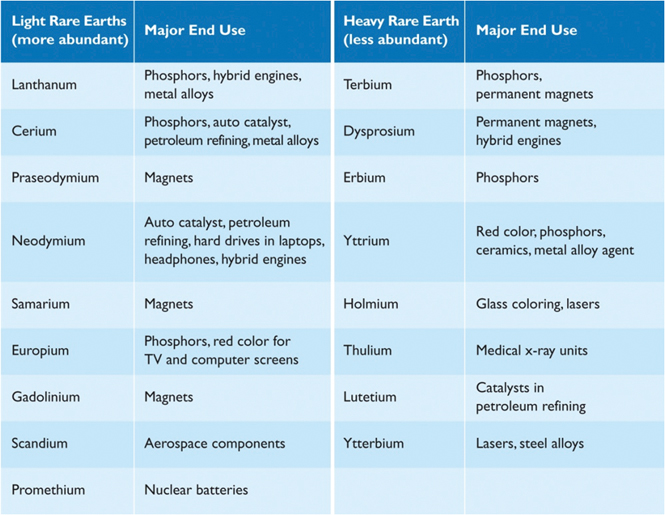
그림 2. 희토류 원소의 주요 용도 (U.S Department of Energy 2010 Critical Materials Strategy Summary.)
Ⅱ. 본 론
Ⅱ-1. 희토류 함유 형광체 기술 현황
일반적으로 형광등, LED 등에 사용되고 있는 형광체는 고상의 무기물 소재로서 주로 불순물이 의도적으로 첨가된 모재(host)로 이루어져 있다. 높은 농도의 불순물을 첨가하면 발광과정의 효율이 감소되기 때문에 첨가된 불순물의 농도는 수% 정도로 낮게 유지된다. 형광체에서의 빛의 흡수 과정은 모재에서 뿐만 아니라 첨가된 불순물에 의해서도 발생하며, 흡수된 에너지는 첨가된 불순물에 의해 발광이 일어나게 되므로, 이를 활성제(activator)라고 부른다.
무기형광체에서 활성제로 사용되는 희토류 원소는 광흡수에 따른 전자의 전이 과정에서 폭이 넓고 강한 발광을 나타내며 모체의 조성을 제어하거나 다른 활성 원소를 도입함으로써 발광특성 조절이 가능하다. 활성제 이온의 광흡수도가 낮은 경우 또다른 불순물이 더 첨가되고 이러한 불순물은 빛을 흡수하고 그 에너지를 활성제에 전달하는 성격을 가지고 있어 증감제(sensitizer)로 일컬어진다(그림 3 참조).
현재 형광체에 사용되고 있는 모재로서는 Y2SiO6, Y3Al5O12 등의 산화물, CaS, SrS, ZnS 등 황화물, CaAlSiN3 등 질화물 또는 산질화물 등이 주류를 이루고 있으며, 주로 La, Y 등 희토류 원소들이 사용되기도 한다. 또한 형광등의 경우 백색 발광을 하는 피로인산칼슘계 ((Ca10(PO4)6F,Cl) 소재가 주요 형광체용 모재로 주로 사용되어 왔다.
한편 활성제의 경우 일부 전이금속이 사용되고 있지만 상업적인 활용성을 가지는 형광체의 대부분 희토류 원소를 활성제로 사용하고 있다. 표 1에는 조명 및 디스플레이에 사용되는 대표적인 형광체와 그들의 발광색을 나타내었다.
형광체를 구성하고 있는 활성제의 전자 에너지 준위 간 천이에 따라 형광체가 발광하게 되며 원리적으로는 진공 중의 이온에서도 발광이 발생할 수 도 있다.
단일 에너지 준위 간 천이에 의해 발생하는 발광은 상온에서도 수 nm 폭의 극히 좁은 발광 파장대역을 가지게 되지만 에너지 준위의 분포가 넓은 에너지대의 경우 가시광선 영역에서 50nm를 초과하는 선폭을 나타내기도 한다.
넓은 발광 스펙트럼은 기저상태와 여기상태의 화학결합 특성 차이가 매우 큰 경우 발생한다. 이러한 넓은 선폭의 발광은 전이금속 이온에서 부분적으로 채워진 d 전자 준위 간의 천이(d→d 천이) 또는 희토류 원소에서 5d 준위와 4f 준위 간의 천이(d→f 천이) 그리고 Tl+, Pb2+, Sb3+ 등 짝지워지지 않은 s 전자를 가지는 이온의 발광에서 주로 발생한다.
반면 좁은 선폭의 날카로운 스펙트럼의 발광은 전자의 화학결합 상태가 기저 상태와 여기상태 간 차이가 적을 때 발생하며 화학결합에 직접 참여하지 않는 전자 상태간 전이 (희토류 원소 이온에서의 f→f 천이)에서 발생한다. 화학결합에 참여하는 전자 상태에서의 광학적 과정에는 결합의 특성 (이온결합성/공유결합성)과 발광 이온이 존재하는 격자 위치 주위의 대칭성 등에 의해 많은 영향을 받는다.
넓은 선폭의 발광을 나타내는 d→d 천이의 예로써 BaMg Al10O17:Mn에서 Mn2+ 이온에 의한 발광을 들 수 있다. 이 형광체에서 발생하는 녹색빛은 전자스핀이 모두 동일 방향인 5d 전자 배치를 가지는 Mn2+ 이온에서 d→d 천이에 의해 발생한다. 이러한 전자 천이는 선택률에 위배되는 금지 전이(forbidden transition)이므로 빛의 흡수도가 낮고 발광의 소광시간이 10ms 정도로 긴 편이다.
한편 희토류 원소의 경우 최외각 전자가 4f shell이고 4f shell의 경우 d shell과 달리 희토류 원소의 특성상 4f shell은 5s나 5p shell에 의해 차폐되어 있어 4f shell은 화학 결합에 직접 참여하지 않으므로 좁은 에너지 분포를 가진다 (그림 7 참조). 따라서 f shell 내에서 발생하는 f→f 천이는 매우 좁은 발광선폭을 나타낸다.
대표적인 예로서 Y2O3:Eu3+는 f 전자 간 천이에 의해 좁은 발광선폭을 나타내는 형광체이다. 4f 전자 간 천이는 앞서 언급한 d→d 천이와 같은 금지 전이 이므로 역시 빛의 흡수도가 낮고 소광 시간은 3ms 정도이다.
이때 좁은 에너지 분포를 가지는 준위 간에 발생하는 발광 과정이므로 발광 과정의 양자효율은 90%에 달하며 주로 고품질 형광등이나 PDP의 녹색형광체로 사용된다. 그러나 본질적으로 희토류 이온에서의 f→f 전이는 전자 전이에 대한 선택률에 위배되기 때문에 발광강도가 낮다는 단점이 있으며, 4f shell의 전자가 결합에 참여하지 않기 때문에 외부 환경에 따른 발광스펙트럼 제어가 어려워 f→f 전이로 발광하는 형광체는 그리 다양하지 않다.
또한 희토류 원소에서 발생하는 중요한 발광 과정에 관여하는 또다른 전자 천이로 5d shell과 4f shell간의 전자 전이(d→f 천이)가 있다. d→f 천이는 넓은 에너지 분포를 가지는 d shell로 여기된 전자가 좁은 에너지 분포를 가지는 f shell로 전이하면서 발광하기 때문에 넓은 발광스펙트럼을 가지게 된다.
대표적인 예가 Y3Al5O12:Ce3+ (YAG:Ce)이다. YAG:Ce 형광체는 우수한 발광성을 가지며 넓은 범위의 황색 발광을 하는 형광체이기 때문에 최근에는 백색 LED의 광변환 소재로 널리 사용되고 있다. YAG:Ce 형광체에서는 4f shell의 전자가 빛 에너지를 받아서 5d shell로 여기되고 이후 다시 4f shell로 천이되며 선택률을 만족하기 때문에 고효율 황색발광을 하게 된다. 또한 d 궤도는 f-궤도에 비해 이온 주위의 환경에 민감하고 이온 주위의 국부적인 환경은 격자 진동에 의해 큰 변화를 받기 때문에 대체로 d 궤도가 포함되는 발광과정에서는 넓은 발광선폭을 가지게 되며 모재의 결정구조 및 조성 등의 제어를 통해 쉽게 발광 파장 영역을 이동할 수 있다.
YAG:Ce 형광체 역시 yttrium을 Tb3+, Gd3+ 등의 중희토류 이온으로 치환하거나 Alumininum을 Mg2+, Si4+로 동시에 치환하면 발광파장이 적색으로 이동하며 Aluminum을 Ga2+ 이온으로 치환하면 청색 방향으로 발광파장이 이동한다. 또한 그림 8에는 대표적인 희토류 원소인 Eu2+ 이온에 대해 모재의 조성 및 결정구조에 따른 발광 파장의 변화를 나타내었다. 모재의 종류에 따라 367nm에서 650nm까지 다양한 발광파장을 가질 수 있어 희토류 이온 주위의 화학적 환경 변화에 따라 발광파장을 조절할 수 있음을 보여준다.
형광체에서 희토류 원소가 많이 사용되는 이유는 크게 아래와 같이 4가지 정도로 요약할 수 있으며, 향후 희토류 원소를 수급이 용이한 타 원소 대체할 경우 희토류 이온의 이러한 장점을 어느 정도 만족시켜야 한다.
(1) 4f shell의 전자는 5d shell과 같이 밴드가 아닌 정해진 준위에 있기 때문에 고효율의 발광이 가능하고, (2) f→f 천이에서 유래하는 뚜렷한 발광이 고연색성을 얻기 위해 유용하다.
(3) Ce3+, Eu2+ 등 d→f 천이를 하는 희토류 이온의 경우 d궤도 에너지준위가 결정구조에 의해 변하기 쉬워 여기, 발광의 에너지를 비교적 간단하게 제어할 수 있다.
(4) 전이금속이온에 비해 원자 가수 제어가 상대적으로 용이하다.
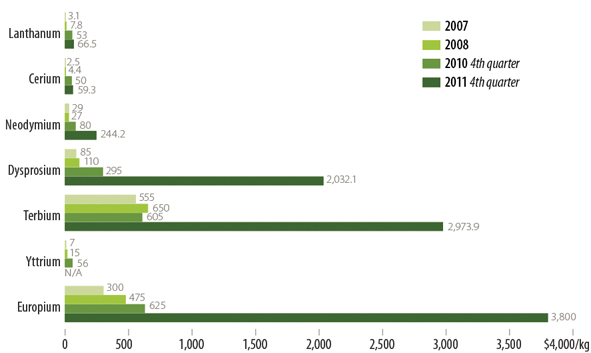
그림 3. 주요 희토류 원소들의 가격변동 추이 (M. Humphries, "Rare earth elements: The global supply chain", Congressional Research Service (2012)) 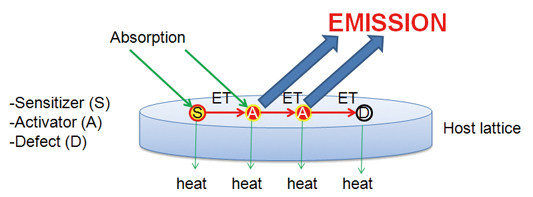
그림 4. 형광체의 구조 및 발광 과정
표 1. 현재 사용되고 있는 다양한 형광체와 그 응용처 
그림 6. 전이금속 원소가 첨가된 형광체 (BaMgAl10O17 doped by 5% Mn2+)의 발광특성
그림 7. 희토류 원소이온의 전자구조
그림 8. 모재 종류에 따른 Eu2+ 이온의 발광 파장의 변화 (좌로부터 SrB4O7, BaMgAl10O17, Ba2SiO4, CaAlSiN3)
Ⅱ-2. 희토류 형광체 대체/저감기술 현황
< 이하 생략- 자세한 내용은 세라믹코리아 2013년 8월호를 참조 바람.>
김 영 국
- 1991~1995 고려대학교 재료공학과 학사
- 1995~1997 포항공과대학교 신소재공학과 석사
- 1997~2002 포항공과대학교 신소재공학과 박사
- 2002~현재 한국기계연구원 부설 재료연구소 선임연구원
기사를 사용하실 때는 아래 고유 링크 주소를 출처로 사용해주세요.
https://www.cerazine.net